La iniciativa crea un Programa de Protección al Personal de Salud ante la pandemia de coronavirus.
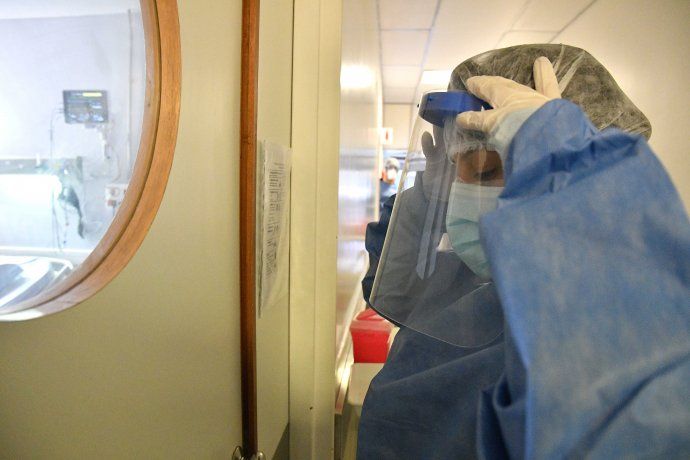
La Ley Silvio recibe su nombre en honor al primer trabajador de salud fallecido por Covid-19 en Argentina, el pasado 18 de abril.
A través de la publicación del DECRETO 747/2020 en el Boletín oficial, el Gobierno reglamentó la “Ley Silvio” una iniciativa para proteger al personal de salud ante la pandemia de coronavirus.
La medida, impulsada por el jefe del Interbloque Federal, Eduardo “Bali” Bucca, médico de profesión, declara de interés nacional la protección de la vida y la salud del personal sanitario durante la epidemia de Covid-19.
Su objetivo principal es la prevención del contagio de coronavirus “entre el personal de salud que trabaje en establecimientos de salud de gestión pública o privada, y entre los trabajadores y voluntarios que presten servicios esenciales durante la emergencia sanitaria”.
Además, establece medidas de bioseguridad en establecimientos de salud, en las áreas específicas dedicadas al tratamiento de casos de Covid-19, así como también protocolos de salud obligatorios, guías de práctica de manejo y uso de insumos para minimizar los riesgos de contagio.
También en su artículo cuarto propone que “sean los trabajadores de menor edad quienes estén a cargo, de forma prioritaria, de la atención de casos sospechosos, toma de muestras, atención y tratamiento de pacientes de Covid-19”, a fin de reducir riesgos entre el personal de mayor edad y más vulnerable al virus.
Por último, se establece la obligatoriedad de la realización de capacitaciones para todo el personal de salud. En caso de aprobarse, la ley tendrá vigencia mientras dure la emergencia sanitaria por el coronavirus.
La “Ley Silvio” recibe su nombre en honor al primer trabajador de salud fallecido por Covid-19 en Argentina, el pasado 18 de abril.
Silvio Cufré tenía 47 años, era enfermero y trabajaba en el Instituto Médico Brandsen, en la provincia de Buenos Aires.
Ese centro de salud del municipio de San Vicente es investigado por la Justicia por irregularidades y violación del protocolo sanitario, tras los primeros casos de coronavirus. Allí, fallecieron el padre y el abuelo del jugador de fútbol, Walter Montillo, pacientes de Cufré, quien los atendió sin saber que tenían coronavirus.
| Fuente: www.ambito.com










:quality(85)//cloudfront-us-east-1.images.arcpublishing.com/infobae/ZNYILIASY2F33VCMII7P5QYYPQ.jpg)
:quality(85)//cloudfront-us-east-1.images.arcpublishing.com/infobae/N42HV3U6QY3EXXK4QSEXGZMMOI.jpg)